
GMP的介绍

GMP是《药品生产质量管理规范》(Good Manufacture Practice, GMP)的英文缩写,是对企业生产过程的合理性、生产设 备的适用性和生产操作的精确性、规范性提出强制性要求。最新版《药 品生产质量管理规范(2010年修订)》已于2010年10月19日经 卫生部部务会议审议通过,现予以发布,自2011年3月1日起正式 施行。
GMP是药品生产和质量管理的基本准则,适用于药品制剂生产 的全过程和原料药生产中影响成品质量的关键工序。大力推行药品 GMP,是为了最大限度地避免药品生产过程中的污染和交叉污染, 降低各种差错的发生,是提高药品质量的重要措施。
目前,在中国生产的药品在全球范围的销售要求制造商不心 符合中国的2010版GMP规范,还要符合国际标准EUIGM FDA-cGMP的要求。
GMP没有详细列出生物洁净室的设计、建造、测试等方面的要求。详细内容还要参照相关的GMP实施指南,药品GMP认证检 评定标准,FED 209E,ISO14644, ISO14698, IEST,国际GBT. EN1822等标准。
洁净室和污染控制技术是保证GMP成功实施的主要手段之一。
生物洁净室相关标准
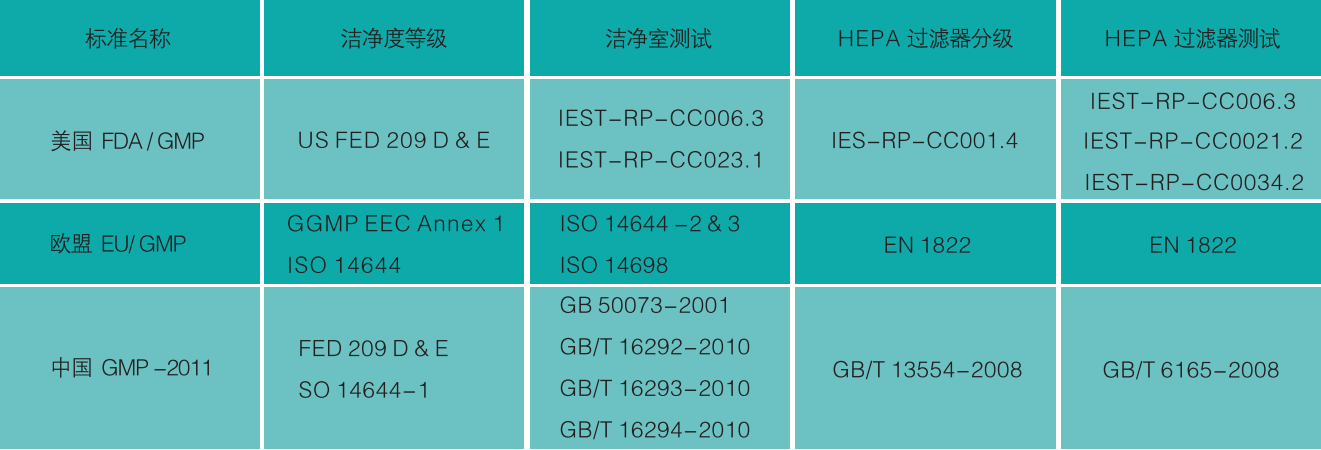
空气的洁净度
生物洁净室空气洁净区分为四个区域:
A级--高风险操作区,即直接影响操 作的区域。像隧道灭菌烘箱、无菌灌装、瓶 子开口处、高压灭菌冷却区等需用100级层 流。直接影响产品质量,称A级。
B级--间接影响无菌操作区,直接环 绕A级区域的地方,像无菌灌装房间、高压
灭菌冷却房间。
C和D级-- 进入无菌生产区的过渡性 洁净区。准备间、更衣间和缓冲间。
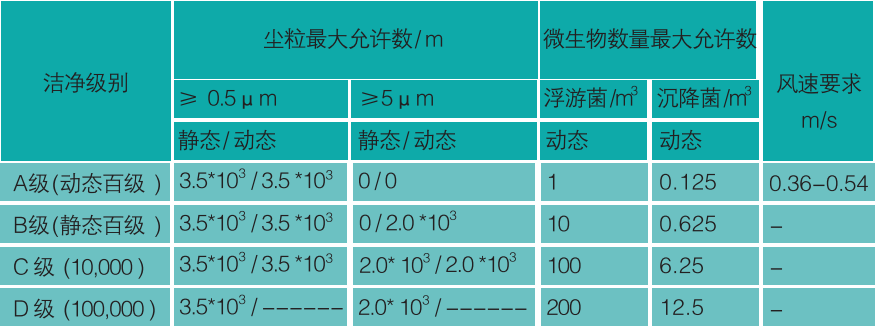
GMP中悬浮粒子分级的不同标准的大致对比
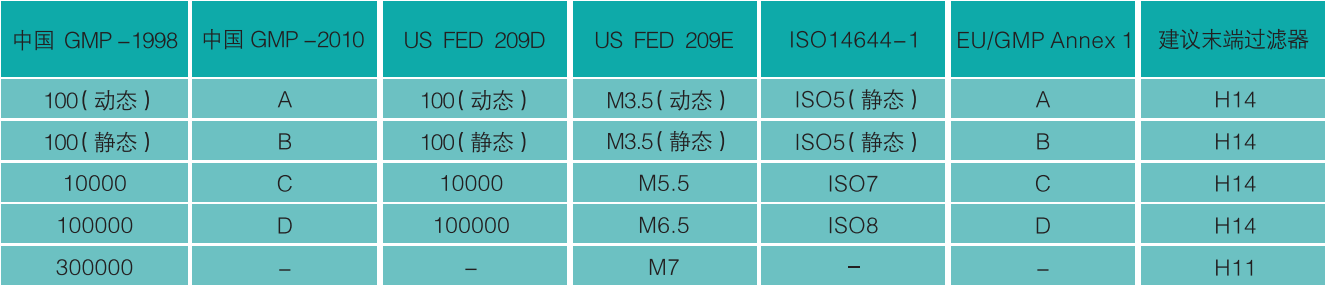
空气过滤器效率规格对比





